KONFERENCE

Pořadatel: 4Education s. r. o. | Záštita: České urologické společnosti ČLS JEP, České akademie urologie, 2. lékařské fakulty Univerzity Karlovy a Fakultní nemocnice v Motole
KOMPLEXNÍ NOVINKY V ONKOUROLOGII
KOMPLEXNÍ NOVINKY V ONKOUROLOGII
Urologické nádory v klinické praxi • Jak postupovat, když nám „guidelines“ nestačí? • Časný záchyt karcinomu prostaty
#rapidKNOU
#rapidKNOU
Archiv příspěvků #rapidKNOU
V rámci letošní online konference jsme pro vás připravili novinku, kterou jsme nazvali #rapidKNOU. Jde o krátké úvahy, tipy a doporučení k léčbě onkourologických nádorů. Od 4. do 21. května budeme každý den publikovat prostřednictvím twitterového profilu @KnouCz a webových stránek konference dvě témata. Nejnovější příspěvky najdete na hlavní stránce webu a všechny ostatní na této archivní.
Edukačním partnerem KNOU 2020 a partnerem rubriky #rapidKNOU je společnost Roche.

Je nutné provést lymfadenektomii (LND) během radikální prostatektomie u 65-letého pacienta s adenokarcinomem prostaty, který má vstupně PSA 16, z biopsie 5 pozitivních vzorků z celkem 8, GS 3+4 (ISUP grade 2) a klinicky T1c nález?
- Dle současných závěrů sice nemá LND během radikální prostatektomie zásadní vliv na onkologický výsledek včetně přežití, avšak zůstává nejspolehlivějším zdrojem informací pro staging onemocnění a pro pacienta může mít důležitý význam při rozhodování o další léčbě – popř. mít i terapeutický benefit.
- Při rozhodování o LND využívejte některý z dostupných nomogramů (např. Briganti 2017, Briganti 2018 – pokud byla předoperačně provedená mpMRI prostaty s pozitivní fúzní biopsií, MSKCC – Memorial Sloan Kettering Cancer Center) – LND indikujte je-li riziko postižení uzlin vyšší než 5% (tento konkrétní případ – Briganti 12%, MSKCC 7%).
- Pokud se rozhodnete o provedení, pak provádějte tzv. eLND (extended lymph node dissection), tedy odstranění lymfatických uzlin z oblasti zevního ilického svazku, z obturatorní fossy nad a pod obturatorním nervem a mediálně a laterálně od vnitřní ilické arterie.
Ondřej Příman
Cystoskopie není zcela dokonalý instrument k diagnostice tumorů močového měchýře a v literatuře se udává, že v 19 až 73% můžeme tumor jednoduše přehlédnout. Přitom prostá cytologie moči nabízí u high-grade uroteliálních tumorů senzitivitu až 84%.
- Je důležité zejména u follow-up pacientů s high-risk NMIBC provádět nejen cystoskopii, ale i odběr cytologie moči- Je důležité zejména u follow-up pacientů s high-risk NMIBC provádět nejen cystoskopii, ale i odběr cytologie moči.
- EAU doporučuje: u pacientů s high-risk NMIBC cystoskopii a cytologii za 3 měsíce. Pokud je výsledek negativní, dále provádět kontrolní cystokopii a cytologii každé 3 měsíce po dobu 2 let, a dále každých 6 měsíců do doby 5 let, poté jednou ročně.
- V případě suspektních lézí je třeba provést jejich biopsii nebo TURB- Nezapomínejte však ani na recidivy v horních močových cestách: u high-risk NMIBC pravidelně jednou ročně doplňte zobrazovací vyšetření- CT IVU.
Martina Tomašov
Jak lze provést en-bloc resekci pomocí kličky nebo incizní elektrody?
-
Incizní elektrodou lze precizně demarkovat okraje tumoru v kombinaci s PDD nebo NBI.
-
Výkon kličkou je bezpečnější vzhledem k přerušované aktivaci proudu a tedy nižším riziku perforace.
-
Retrográdní technika s využitím kličky je výhodnější v situacích, kde na počátku resekce není dostupný zadní okraj tumoru.
Marko Babjuk
Intravezikální léčba BCG je obvykle dobře tolerována. Relativně nezávažné nežádoucí účinky, které vymizí během několika hodin nebo dní po aplikaci, se objevují u 69,5 až 91 % pacientů a bývají především lokální (dysurie, hematurie) a mírné celkové (subfebrilie, únava, nevolnost, zimnice, malátnost). U méně než 5% pacientů může vést intravezikální podání BCG vakcíny k závažným komplikacím, vč. pneumonitidy, hepatitidy, sepse a dokonce i smrti.
- Nepodávejte intravezikální léčbu BCG dříve než 2 týdny po transuretrální resekci, při traumatické katetrizaci před instilací a při makrohematurii, dále pacientovi se symptomy infekce močových cest či imunosuprimovanému jedinci (leukémie, infekce HIV, terapie imunosupresivy, st.p. transplantaci apod.).
- Pacientům s několikadenními příznaky cystitidy někdy provázenými teplotou do 38°C odložte aplikaci BCG vakcíny, odeberte kultivaci moči a zahajte empirickou léčbu antibiotiky pokrývající gramnegativní bakterie. Terapie fluorochinolony může být navíc účinná i proti mykobakteriím.
- Při závažnějších symptomech jako je febrilie nad 38,5°C a při výskytu nespecifických flu-like příznaků (únava, malátnost, zimnice) trvajících déle než 2 dny pomýšlejte na systémovou infekci BCG. Odeberte hemokultury, moč na kultivaci a proveďte vyšetření plic pomocí RTG, či lépe CT hrudníku.
- Při infekci vyvolané BCG nepodávejte antituberkulotikum pyrazinamid, na které je M. bovis primárně rezistentní.
Barbora Nechanská
Některé recidivy nádorů močového měchýře je možné dle doporučení EAU pouze ambulantně koagulovat.
- Týká se to pacientů s anamnézou Ta LG/G1 nádorů- Týká se to pacientů s anamnézou Ta LG/G1 nádorů.
- Recidivy musí být drobné (do 5-10 mm), papilárního charakteru, dobře ohraničené (zkušený urolog je do značné míry schopen predikovat grade nádoru dle jeho vzhledu) a uložené v části měchýře bezpečně dostupné pro koagulaci.
- Pro zajímavost, v indikovaných případech, zvláště u starších a polymorbidních nemocných, je možné takové recidivy dokonce jen sledovat.
Jakub Horňák
Multiparametrická magnetická rezonance prostaty jako zobrazovací metoda v detekci karcinomu prostaty má senzitivu 91 % a specificitu 37 % (pro ISUP grade ≥ 2 CaP).
- I když nám mpMRI pomáhá snížit počet biopsií prostaty jakožto invazivního vyšetření, nezapomínejte, že mpMRI prostaty sama o sobě není diagnostická, ale pomocná metoda.- I když nám mpMRI pomáhá snížit počet biopsií prostaty jakožto invazivního vyšetření, nezapomínejte, že mpMRI prostaty sama o sobě není diagnostická, ale pomocná metoda.
- Neměl-li pacient v minulosti biopsii prostaty, je možné provést mpMRI prostaty před plánovanou biopsií, která vám pomůže v dalším rozhodování. V případě pozitivního výsledku (t.j. PIRADS skóre ≥ 3 ) doplňte cílenou i systematickou biopsii prostaty. V případě negativního výsledku (t.j. PIRADS skóre ≤ 2 ) a nízkého podezření na karcinom prostaty je možné biopsii prostaty vynechat za dalšího pravidelného sledování pacienta.
- Měl-li pacient v minulosti systematickou biopsii s negativním histologickým výsledkem a trvá podezření na karcinom prostaty, je doporučeno mpMRI doplnit. Je-li výsledek pozitivní (t.j. PIRADS skóre ≥ 3 ), měl by pacient podstoupit biopsii prostaty. Je-li výsledek negativní (t.j. PIRADS skóre ≤ 2 ) a trvá podezření na karcinom prostaty, je doporučeno provést systematickou biopsii prostaty.
- EAU doporučuje u všech pacientů s podezřením na karcinom prostaty provést její systematickou biopsii, není-li mpMRI dostupná.
Martina Tomašov
35 % pacientů s nádorem pT2N0 a 40 % pT3N0 umírá po radikální cystektomii v důsledku progrese nádoru. Až 80 % recidiv je v podobě vzdálených metastáz.
- Snažte se během radikální cystektomie dosáhnout negativních chirurgických okrajů, provést adekvátní lymfadenektomii.
- Indikujte neoadjuvantní chemoterapii u pacientů únosných k aplikaci cisplatiny, tento postup snižuje o 14% riziko úmrtí na nádor měchýře.
- Sledujte nové trendy, které mohou v budoucnu výsledky zlepšit. Neoadjuvantní aplikace atezolizumabu (ABACUS study) a pembrolizumabu (PURE-01 study) dosáhla kompletní remise u 31 % a 42 % léčených. Budoucnost přinese i lepší výběr konkrétního postupu díky využití biomarkerů a molekulární klasifikace konkrétního tumoru.
Marko Babjuk
Až 10 % pacientů v aktivním sledování pro nízce rizikový karcinom prostaty začne trpět strachem z dalšího sledování.
Obavy pacienta z prodlení by měly vést k detailnímu pohovoru:- Obavy pacienta z prodlení by měly vést k detailnímu pohovoru:
- připomeňte, že přibližně 1/3 pacientů v režimu aktivního sledování dospěje k aktivní léčbě a onkologické výsledky (zatím jen 5leté) radikální prostatektomie na začátku sledování a po nějaké době sledování (medián 3 roky) se nelišily.
- Zároveň objasněte možné riziko, vyplývající z aktivního sledování – v horizontu 10 let lehce zvyšuje oproti aktivní léčbě už tak malé riziko metastazování (z 2.6 na 6% – studie PROTECT) – avšak sledování ve studii PROTECT využívalo pouze PSA, takže lze předpokládat, že při současném používání moderních metod jako je mpMRI ( a snad brzy u nás i genomové markery) bude toto riziko ještě nižší.
- Samotné zvýšení PSA (speciálně PSA-DT <3 roky) není dostatečný indikátor pro změnu, mělo by však iniciovat opakování mpMRI prostaty a biopsii- změna na kontrolním mpMRI prostaty by měla vést ke konfirmační biopsii, nikoliv rovnou k indikaci aktivní léčby.
- Přetrvávající pacientovy obavy z aktivního sledování by měly být indikací ke změně terapeutického postupu.
Ondřej Příman
Až 50 % nemocných s plicní recidivou po RCYE nebo NEU může přežívat 5 let po metastazektomii.
- Oligometastatické onemocnění je koncept definováný jako omezený počet nádorových lézí mimo močový měchýř (extraregionální uzliny, orgánové metastázy), který lze ovlivnit lokální ablační léčbou.
- Primárně je vždy indikována systémová léčba (indukční chemoterapie, imunoterapie), ať už se jedná o primárně oligometastatické onemocnění nebo recidivu uroteliálního karcinomu po předchozí kurativní léčbě.
- Při dobré odpovědi může část pacientů profitovat z lokální kontroly, tedy tzv. konsolidační cystektomie nebo radioterapie; ve vybraných případech lze zvážit i metastazektomii; podstatným faktorem je dobrý PS.
- Salvage cystektomie je metodou volby k prevenci nebo řešení lokálních komplikací (hematurie, bolest, obstrukce) .
Antonín Brisuda
U mužů po radikální cystektomii s ortotopickou neovezikou je dle literatury riziko recidivy uroteliálního karcinomu v uretře 2,2 %.
- Pokud zvažujeme ortotopickou náhradu močového měchýře, je nutné peroperační histologické vyšetření z resekčního okraje uretry. V případě pozitivního nálezu je nezbytné spolu s cystektomií provést uretrektomii a jiný typ derivace.- Pokud zvažujeme ortotopickou náhradu močového měchýře, je nutné peroperační histologické vyšetření z resekčního okraje uretry. V případě pozitivního nálezu je nezbytné spolu s cystektomií provést uretrektomii a jiný typ derivace.
- U mužů, u kterých nevyužíváme uretru k derivaci moči (např. při ureteroileostomii), je riziko sekundárního uroteliálního karcinomu v ponechané močové trubici dle některých prací dokonce vyšší – až 5,5 %. Platí proto stejné doporučení o peroperační biopsii a uretrektomii jako u ortotopické náhrady.
- Při ponechané močové trubici je třeba ji dále sledovat pomocí cytologického vyšetření moči (u ortoepické náhrady) nebo výplachu z uretry (u ureteroileostomie).
- V indikovaných případech doplňujeme i uretroskopii.
Richard Ondrejček
Věk a předoperační stav erekce jsou nadále důležitými faktory pro závažnost erektilní dysfunkce po radikální prostatektomii.
- Snažte se o provedení nervy-šetřícího výkonu u indikovaných pacientů, zachování nervově-cévních svazků může mít pozitivní vliv na pooperační erektilní funkci.
- Lepší stav kontinence po nervy-šetřící radikální prostatektomii je pravděpodobně vázán na pečlivou preparaci apikální oblasti prostaty, která se k tomuto výkonu pojí.
- Zvažte vynechání nervy-šetřícího výkonu u pacientů s cT2c nebo cT3 nálezem a ISUP grade >3 karcinomem.
Ondřej Příman a Tereza Zdobinská
Je v dnešní době a moderních přístupech (robotická chirurgie) nadále stejné riziko močové inkontinence po chirurgické léčbě karcinomu prostaty?
- Přestože některé studie ukazují, že funkční komplikace při srovnání otevřené a roboticky asistované prostatektomie jsou v horizontu 12 měsíců srovnatelné, má robotická prostatektomie nižší riziko pooperačních komplikací a ze zkušeností z našeho pracoviště jsou funkční výsledky minimálně v časném období příznivější oproti otevřeným výkonům.
- U pacientů s BMI>30 očekávejte dobu dosažení močové kontinence dvojnásobnou. Rozhodujícím faktorem dosažení kontinence je však věk pacienta.
- Předoperační provádění cviků na posílení svalů pánevního dna může mít pozitivní efekt na následnou restauraci kontinence.
- Sledujte dlouhodobé pooperační funkční výsledky u svých pacientů na vašem pracovišti.
Ondřej Příman a Tereza Zdobinská
Jak volíme derivaci moči po cystektomii? Dle dat prezentovaných na EAU2019 bylo ve Španělsku provedeno 19 % ortotopických neovezik, 1 % kutánních ureterostomií a 80 % ureteroileostomií.
- Pečlivá konzultace operatéra s pacientem je samozřejmostí
- Je třeba zohlednit preference pacienta, ale ten musí znát výhody a nevýhody jednotlivých typů derivací (rizika, kvalita života atd.)
- Ortotopická (ev. heterotopická) náhrada měchýře předpokládá dobrý kognitivní stav pacienta a jeho jasnou motivaci, dobrou funkci ledvin a jater, a zkušenost operatéra a pracoviště
- Onkologický rozsah (postižení uzlin, uretry apod.) a anatomické poměry v břiše, pánvi a uretře jsou klíčovými faktory při definitivním rozhodování; pacient musí být dobře infomován a podepsat IS se všemi možnými alternativami, které mohou vyvstat až v průběhu operace
Antonín Brisuda
Muž ve věku 75 let s PSA 5.2 ng/ml má dle PCPT kalkulátoru riziko klinicky signifikantního karcinomu prostaty 11 %. Má smysl mu provádět biopsii prostaty?
- Zhodnoťte pacientův celkový zdravotní stav a očekávané přežití (lze využít některé skórovací systémy, například G8 či mini-COG) nebo dokonce online risk kalkulátor kombinující údaje o prostatě a komorbiditách (https://riskcalc.org/ProstateCA_Screen_Tool/).
- Opakujte test PSA (hodnoty PSA se mohou v čase i mezi laboratořemi lišit a mohou být ovlivněny různými faktory, například infekcí močových cest).
- Využijte pomocné biomarkery (fPSA a PHI zvyšují specificitu celkové hodnoty PSA především při PSA 4-10 ng/ml o 10-20%, resp. 10-25%).
- Doplňte mpMRI – má až 88% negativní prediktivní hodnotu a to především u případů s obecně nižším rizikem přítomnosti karcinomu.
- U tohoto pacienta (per rectum normální nález, objem prostaty 40g) snižuje negativní MRI nález (PIRADS 2) riziko klinicky signifikantního karcinomu prostaty ve SWOP online kalkulátoru na 3%!
Vojtěch Novák
Riziko úmrtí na T1G3 nádor močového měchýře v průběhu 5 let je přes léčbu BCG vakcínou je 11.3 %.
- U nejrizikovější skupiny (mnohočetný a plošně rozsáhlý nádor T1G3, T1G3 provázený Tis v měchýři nebo prostatické uretře, přítomnost některých aberantních histologických typů) navrhněte pacientovi i možnost okamžité cystektomie.
- Rozhodnete-li se pro BCG, pak ji podávejte v nejúčinnějším režimu, tedy včetně „maintenance“ po dobu 1 roku.
- Pečlivě sledujte pacienty v průběhu léčby (cystoskopie, cytologie moči a 3 měsíce, biopsie a TURB u suspektních nálezů).
- V případě recidivy splňující definici „BCG unresponsive“ (viz EAU Guidelines) neváhejte včas indikovat radikální cystektomii.
Marko Babjuk
69letý pacient s anamnézou resekce levé ledviny pro karcinom přichází s nálezem oboustranného tumoru ledviny. Dle CT je vlevo v dolním pólu suspektní ložisko o velikosti 24 x 28 mm, pro nejasný vzhled ložiska horního pólu pravé ledviny byla navíc doplněna NMR, dle které vyslovena též suspekce na malignitu.
Jak byste postupovali u tohoto pacienta? Změnil by se Váš přístup u pacienta se syndromem VHL?
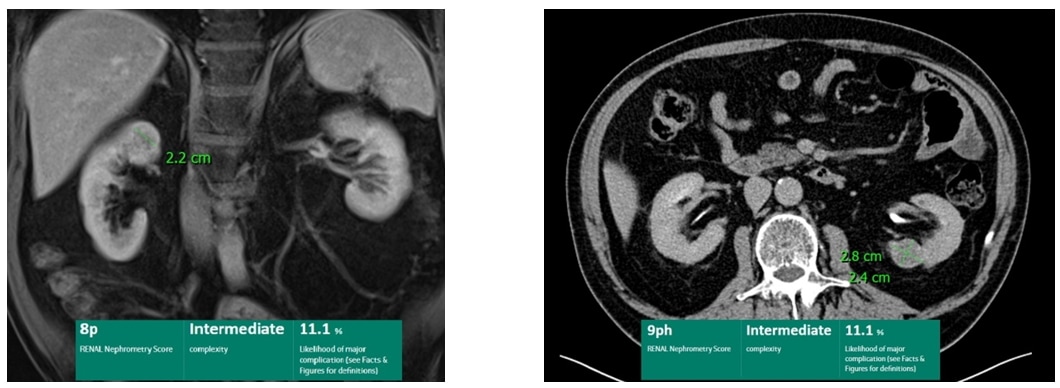
Vzhledem k vyšší suspekci jsme zvolili nejprve otevřenou resekci vlevo s histologickým závěrem světlobuněčný karcinom (grade 2). Následně jsme přistoupili k resekci vpravo se stejným histologickým výsledkem.Vzhledem k vyšší suspekci jsme zvolili nejprve otevřenou resekci vlevo s histologickým závěrem světlobuněčný karcinom (grade 2). Následně jsme přistoupili k resekci vpravo se stejným histologickým výsledkem.
Poznámky:
- Závěry dostupných studií synchronních bilaterálních tumorů ledvin naznačují, že nález maligního nádoru na jedné straně představuje vysoké riziko malignity i v kontralaterální ledvině (84 – 95%). Oproti tomu nález benigního ložiska v první histologii predikuje nález benigního tumoru i na druhé straně v menší míře (39 – 67%).
- Vzhledem k T1a stadiu je preferovanou metodou u takového pacienta bilaterální parciální nefrektomie.
- U pacienta se syndromem VHL je vzhledem k vysokému riziku recidivy renálního karcinomu doporučováno ložiska do 3 cm sledovat, přičemž cílem je zabránit vzniku metastatického onemocnění při co nejdelším zachování renálních funkcí.
Barbora Žemličková
Až tři čtvrtiny pacientů s perzistentním PSA po radikální prostatektomii (definováno jako PSA ≥ 0.1 ng/ml 4-6 týdnů po operaci) dosáhnou biochemické recidivy a jejich pravděpodobnost 10-ti letého přežití je nižší o 20%.
- Nezapomínejte, že PSA je stále nejcitlivější ukazatel onkologického úspěchu operace. – Nezapomínejte, že PSA je stále nejcitlivější ukazatel onkologického úspěchu operace.
- Nabírejte první pooperační PSA v intervalu 4 – 6 týdnů navzdory obecnému doporučení EAU (první pooperační kontrola PSA až ve 3 měsících).
- Máte-li měsíc po operaci v ruce histologii s některou z negativních prognostických známek (pozitivní chirurgické okraje, GS ˃7, pT3, N+) podpořenou ještě perzistentním PSA – neváhejte a pacienta směřujte co nejrychleji k agresivní sekundární terapii
Štěpán Veselý
Publikovaná retrospektivní studie zaznamenala u pacientů se středně a vysoce rizikovým NMIBC, kteří nebyli léčeni BCG vzhledem k její nedostupnosti, významně vyšší riziko recidivy (46,9% vs 16,2%) a nárůst počtu pacientů podstupujících cystektomii.
- Vzhledem k nedostatku BCG vakcíny přistupujte ke každému pacientovi s NMIBC individuálně a pečlivě zvažujte indikaci každé intravezikální léčby. – Vzhledem k nedostatku BCG vakcíny přistupujte ke každému pacientovi s NMIBC individuálně a pečlivě zvažujte indikaci každé intravezikální léčby.
- Pokud se rozhodnete pro intravezikální terapii BCG, podávejte vakcínu ve standardním režimu po dobu 1 roku (indukční 6-týdenní režim + 3-týdenní instilace ve 3., 6. a 12. měsíci), nesnižujte počet intravezikálních instilací a neredukujte jednotlivé dávky BCG terapie.
- Při nedostupnosti BCG vakcíny je alternativní léčbou pro pacienty se středně rizikovým NMIBC intravezikální chemoterapie mitomycinem či epirubicinem.
- Pacientům s high risk NMIBC můžete doporučit též intravezikální chemoterapii, kterou lze potencovat pomocí experimentálních metod, jako je technologicky asistovaná instilace (např. termochemoterapie).
- U pacientů s nejrizikovějším NMIBC (současně se vyskytující T1G3/HG a CIS v močovém měchýři či prostatické uretře; vícečetný, rozsáhlý nebo recidivující T1G3/HG; aberantní histologické varianty uroteliálního karcinomu; LVI) zvažte časné provedení radikální cystektomie.
Barbora Nechanská
„Pane doktore, zjistili mi nádor a chtějí mi odstranit měchýř? Mám jít na robota?“
- Riziko pooperačních komplikací a onkologických výsledků při radikální cystektomii je při otevřeném či miniinvazivním provedení srovnatelné. Dokládají to výsledky studií CORAL (3 ramenná studie z jednoho centra srovnávající otevřený, laparoskopický a robotický výkon) i RAZOR (multicentrická studie srovnávající otevřený a robotický výkon).- Riziko pooperačních komplikací a onkologických výsledků při radikální cystektomii je při otevřeném či miniinvazivním provedení srovnatelné. Dokládají to výsledky studií CORAL (3 ramenná studie z jednoho centra srovnávající otevřený, laparoskopický a robotický výkon) i RAZOR (multicentrická studie srovnávající otevřený a robotický výkon).
- Klíčová je zřejmě zkušenost operatéra i pracoviště – guidelines EAU doporučuji provedení alespoň 10, ideálně 20, radikálních cystektomií za rok. Z dat z České Republiky víme, že riziko fatálních komplikací během 90 dní po výkonu bylo o více než 5% vyšší u pracovišť s méně než 5 provedenými cystektomiemi ve srovnání s pracovišti s více než 20 provedenými výkony.
- Volba konkrétního přístupu by měla respektovat zkušenosti daného pracoviště a operatéra.
- Pacient by měl být o výhodách i nevýhodách jednotlivých postupů informován.
Michal Nekula
Salvage radioterapii po radikální prostatektomii indikujeme i u některých pacientů, kteří ještě nedosáhli konvenční hranice biochemické recidivy 0.2 ng/ml.
Typický příklad:
RRP+LE 6.9.2016
pT2a, pN0, PN1, L0, R0, GS 4+3
21.09.2016-0,137
05.10.2016-0,022
02.11.2016-0,009
30.11.2016-0,007
01.03.2017-0,005
06.09.2017-0,008
06.12.2017-0,014
07.03.2018-0,013
06.06.2018-0,016
19.09.2018-0,021
09.01.2019-0,031
10.04.2019-0,033
10.07.2019-0,063
09.10.2019-0,063
08.01.2020-0,084
08.04.2020-0,112
Indikace k SRT
- K pooperačnímu monitorování PSA používejte test s citlivostí do 0.01 ng/ml (dříve nazývaný „ultrasenzitivní“), který je již běžně dostupný ve většině laboratoří
- Při takto detailním sledování je v popisovaném případě zřejmý graduální nárůst PSA s Doubling-time ˂ 1 rok, což společně s ISUP 4 řadí dle současné klasifikace EAU pacienta do skupiny „High-Risk BCR“
- Čím dříve indikujete „High-Risk BCR“ pacienta k salvage radioterapii, tím lepší efekt léčby můžete očekávat! Bylo prokázáno, že účinnost salvage radioterapie klesá, pokud je aplikována u pacientů s PSA nad 0,5 ng/ml (doporučení EAU). V naší vlastní studii (Ces Urol 2012, 16(2):92-100) jsme demonstrovali, že aplikace radioterapie při hodnotách PSA do 0,2 ng/ml měla 95% šanci na dlouhodobý úspěch, zatímco hodnoty PSA 0,2-0,3 ng/ml jen 55% šanci.
Ladislav Jarolím
Riziko neúplné resekce (perzistence onemocnění) po TURB pro nádor klasifikovaný jako T1 je dle literatury cca 50 %.
- Guidelines EAU doporučují u všech nádorů T1 za 2-6 týdnů druhou dobu resekce (reTURB).
- Snažte se ale současně zlepšit výsledky úvodní resekce, zvažujte její techniku (např En-bloc resekce), využívejte moderní zobrazení (NBI, PDD), sledujte procento přítomnosti svaloviny u vámi prováděných výkonů.
- Hodnoťte a registrujte výsledky TURB prováděných na vašem pracovišti (procento pozitivních nálezů při reTURB, procento časných recidiv po TURB), srovnejte je s publikovanými výsledky.
Marko Babjuk
U 52-letého pacienta s PSA 7.9 ng/ml, který se s ničím neléčí, je sexuálně aktivní, kontinentní a dobře spolupracující, byl při biopsii prostaty identifikován adenokarcinom ISUP grade 1 ve 4 ze 14 vzorků, kdy nádor postihoval až 60% bioptické tkáně. Bude u takového pacienta možné zvolit aktivní sledování jako adekvátní postup?
- Zmíněný pacient splňuje kritéria zařazení do aktivního sledování (AS) na základě mezinárodního konsensu DETECTIVE Study Eur Urol 2019.
- Pro zařazení pacienta do AS je třeba splnit několik podmínek:
- Předpokládaná délka života >10 let
- ISUP grade 1, klinicky <T2a, PSA <10 ng/ml (popř. PSA denzita <0.15 ng/ml/cm3)
- Nově zde již nebereme ohled na množství pozitivních vzorků při biopsii ani procentuální zastižení nádoru ve vzorku
- ISUP grade 2, klinicky <T2a, PSA <10 ng/ml a nízký počet pozitivních vzorků
- Neměli bychom zařadit pacienty:
- ISUP grade 3 a více
- Pokud je v bioptickém vzorku převládající duktální karcinom, sarkomatoidní karcinom, malobuněčný karcinom nebo přítomnost extraprostatického šíření či lymfangioinvaze
Ondřej Příman
Jednorázová pooperační instilace chemoterapeutika do močového měchýře může být indikována i u vybraných neinvazivních nádorů ve středně rizikové skupině.
- Středně riziková skupina pacientů je vymezena negativní definicí, tj. ti co nespadají do nízce a ani do vysoce rizikové skupiny. Zjednodušeně se jedná o recidivy a/nebo vícečetné povrchové tumory nízkého gradu (LG).
- V době rozhodnutí o instilaci musíme vycházet z dostupných údajů, protože informaci o hloubce invaze a gradu v tuto chvíli nemáme. K instilaci např. indikujeme pacienty s primárními mnohočetnými menšími papilárními tumory nebo pacienty s papilární recidivou/recidivami a s intervalem delším než 1 rok od předchozí recidivy. Studie prokázaly, že u takových pacientů lze snížit 5tileté riziko recidivy až o 14%.
- Riziko progrese a z toho plynoucí riziko úmrtí na karcinom močového měchýře nejsou jednorázovou instilací ovlivněny.
- Na rozdíl od skupiny s nízkým rizikem by u středně rizikových nádorů měla následovat kúra opakovaných instilací.
Jakub Horňák
Riziko recidivy lokalizovaného karcinomu ledviny u pacientů po pěti letech od nefrektomie či resekce ledviny je 2 – 10%.
- Stratifikujte pacienty do rizikových skupin pomocí dostupných skórovacích systémů, např. UCLA Integrated Staging System (UISS) for RCC (https://www.mdcalc.com/ucla-integrated-staging-system-uiss-renal-cell-carcinoma-rcc#use-cases). Např. 5letého celkového přežití (OS) dosáhne 91 % pacientů (ECOG PS 0) s renálním karcinomem I. stádia.
- Zvláště u pacientů se zhoršenou funkcí ledvin před nebo po operaci sledujte renální funkce stanovením kreatininu v séru a odhadem glomerulární filtrace (eGFR). Zpřísněte sledování pacientů po nefron-šetřících výkonech u nádorů větších 7 cm nebo při pozitivních chirurgických okrajích.
- K vyloučení plicních metastáz dejte přednost počítačové tomografii před rentgenovým snímkem.
- U nádorů s nízkým rizikem přizpůsobte intervaly sledování s ohledem na dávku záření a přínos vyšetření.
Barbora Nechanská
Jak zvolit nejvhodnější postup u pacienta se svalovinu infiltrujícím nemetastatickým nádorem močového měchýře?
- U nejasných histologických nálezů neváhejte kontaktovat patologa a eventuelně si vyžádejte druhé čtení, pokud se jedná o nález z jiného pracoviště; variantní histologie uroteliálního karcinomu může zásadně změnit přístup a doporučení.
- Nezbytností je provedení kompletního stagingu onemocnění pomocí CT-IVU a CT plic; bimanuálním vyšetřením pánve posoudíme lokální rozsah a tedy operabilitu; scintigrafii skeletu indikujeme pouze v případě symptomtologie.
- Vždy je třeba respektovat přání pacienta, nicméně pacient musí znát rizika a výsledky různých postupů, rizika prodlení v léčbě, ale také Vaše zkušenosti a výsledky.
- Zhodnoťme celkový zdravotní a biologický stav nemocného, jeho fyzické rezervy; neváhejte konzultovat klinického onkologa v rámci KOC.
- Pokud se rozhodnete pro radikální cystektomii, zvažujte také únosnost neoadjuvatní systémové chemoterapie s cis-platinou.
- V individuálních případech po maximální resekci nádoru může pacient profitovat z kombinované onkologické léčby (chemoterapie a radioterapie), která je také metodou volby u velmi rizikových nemocných (polymorbidita, extremní obezita apod.).
Antonín Brisuda
U 31 % pacientů s low-risk karcinomem močového měchýře dojde během prvních 5 let po iniciální TURB k recidivě. Pokud se však recidiva do této doby neobjeví, s 98,3% pravděpodobností k ní nedojde ani za dalších 15 let.
- Prognosticky je velmi důležitý výsledek první cystoskopie po 3 měsících. Dle guidelines EAU i AUA je proto nezbytné provedení cystoskopie 3 měsíce po TURB.
- Pacienti s low-risk tumorem mohou mít potom další cystoskopii až za 6-9 měsíců a následně jednou ročně po dobu pěti let. Zda a s jakou frekvencí mají být prováděny cystoskopie poté, je předmětem diskuze.
- Naopak pacienti s high-risk tumory by měli podstupovat cystoskopii s cytologií jednou za 3 měsíce po dobu dvou let, následně tři roky každých 6 měsíců, dále pak jednou ročně. I po 5 letech je v této skupině nezanedbatelné riziko recidivy a progrese, proto bývá dlouhodobá dispenzarizace nezbytná.
Kateřina Dušková
ZDE SE MŮŽETE PTÁT NEBO PŘISPĚT SVÝM NÁZOREM
ZDE SE MŮŽETE PTÁT NEBO PŘISPĚT SVÝM NÁZOREM
Vyplnění políčka se jménem není povinné. Každý komentář je zobrazen až po schválení moderátorem.

Bez komentářů